QARA
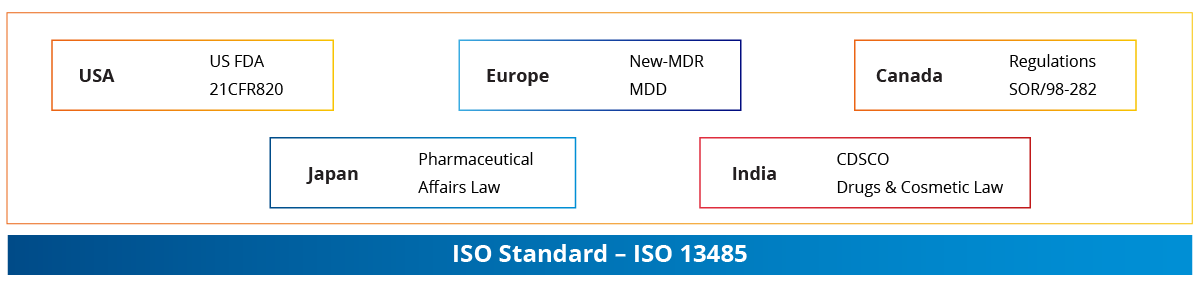
医療機器業界は急速に変化しています。OEMは競争力の維持と生存のために新製品の発売、新規市場への参入、複数のQRAガイドラインの遵守に追われています。しかし、規制の複雑化と国による規制や要件の差異は、多くのOEMにとって大きな障壁となっています。
LTTS事業概要
x
 コンプライアンス
コンプライアンス
- DHF(設計履歴ファイル)の文書化と修正
- UDIの実装
- QMSの更新
- RoHS指令 / REACH規則
- リスク管理文書の作成
x
 製品とプロセス
製品とプロセス
- RCA(原因分析)とCAPA(是正措置・予防措置)
- CDP文書の作成
- DHF(設計履歴ファイル)利便性の向上
- 製造作業指示書の作成
- 生産工程転送サポート
x
 検証
検証
- 設計の検証と妥当性確認
- テストメソッドバリデーション(TMV)
- プロセスの検証
- コンピュータ化システムバリデーション(CSV)
- 成分検定
- サプライヤー変更管理
規制に関する専門知識

診断
体外診断用医薬品

デジタルヘルス

外科

整形外科
LTTSが選ばれる理由

社内インフラ
当社の社内施設は、EMI / EMC、振動、衝撃、環境チャンバー、および材料試験ラボでR&Dおよび革新を支援します

認定ソリューション
ISO 13485:2016とISO9001:2008認証を取得したLTTS品質管理システム

コンサルティングサポート
UL、CSA、ATEX等の品質システム認定証明書を専門とする認定機関やコンサルタントとの提携による、サービスの強化

提携ネットワークの拡張
SGS、TUV、インターテック等の検査、検証、試験、認証を専門とする大手企業を含めたパートナーエコシステム
リソース
パンフレット
ケーススタディ
PoV