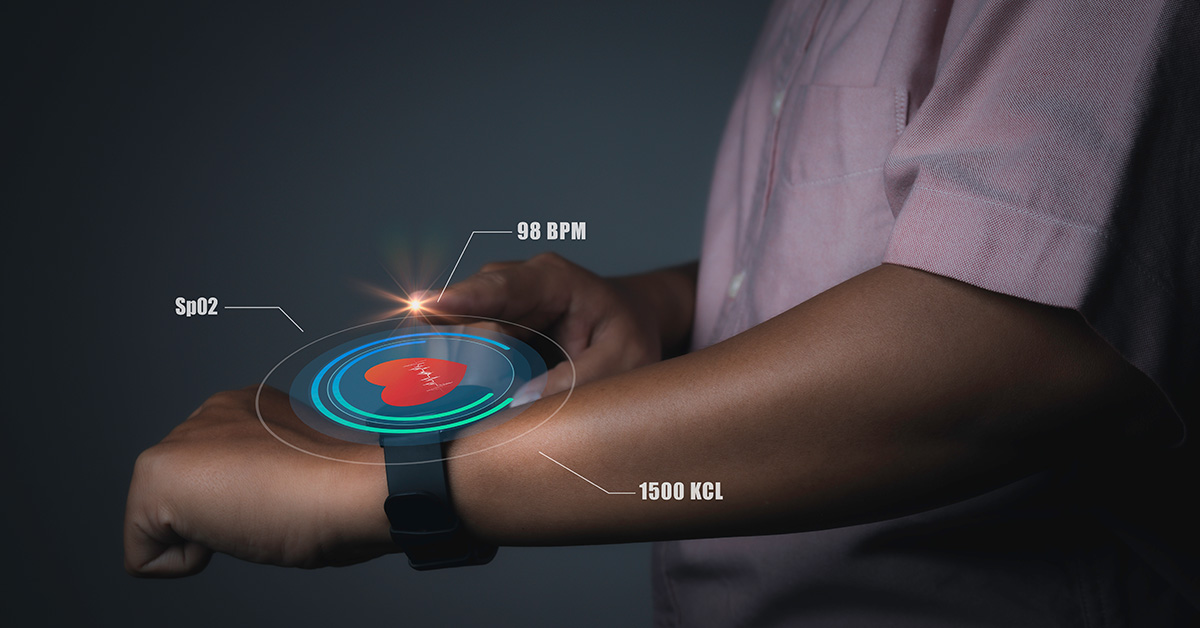
現代の医療施設では、テクノロジーの普及が一目瞭然だ。予後や診断から患者のモニタリングや治療の実施に至るまで、幅広いソフトウェア対応機器により、医療従事者はそれぞれの職務をタイムリーかつ正確に遂行することができます。つまり、医療機器に搭載されるソフトウェア(SiMD)は、医療機器そのものと同じくらい重要なコンポーネントなのです。医療機器内に存在しないが、医療目的で使用されるソフトウェア・ソリューションは、医療機器としてのソフトウェア(SaMD)と呼ばれる。驚くことではないが、これらの驚異的な技術はいずれも、医療機器に適用される厳しい規制ガイドラインに該当する。
SiMDもSaMDも、使用される国の医療機器規制の対象となる。例えば、米国では食品医薬品局(FDA)、欧州では欧州委員会、シンガポールでは保健科学庁(HSA)である。ほぼすべての国にSaMDの規制基準があるが、国の内情や医療に対する考え方によって規制は異なる。そのため、SaMDプロバイダーは、国際的な規制基準であり、多くの国で受け入れられているIEC 62304:2006を遵守しなければならない。
IEC 62304はすべてのライフサイクルプロセスに適用されます。すべてのSiMD開発者はこれに準拠しなければならない。IEC 62304ガイドラインでは、SiMDを安全性に基づいて3つのカテゴリーに分類している:A、B、Cである:
クラスAのSiMDは、患者にとって危険でないものを対象としている。たとえハザードを引き起こしたとしても、ソフトウェアの外部で適切なリスク管理措置がとられていれば、その状況が許容できないリスクにつながることはない。パンデミック以降に急増したさまざまなCOVID-19診断キットは、クラスA SiMDの適切な例である。サンプルを分析するソフトウェアが誤動作し、不正確な結果が出たとしても、ユーザーに直接的な危害を与えることはなかった。結果が正確であったなら、利用者は薬物療法に頼っただろう。
クラスBのSiMDは、ソフトウエアの外部で適切なリスク管理措置を講じた後でも、許容できないリスクを引き起こす危険性があるが、その結果起こりうる危害は重傷ではない。例えば、X線への過度の被曝は人体に有害である。しかし、X線を照射するためのソフトウェアが誤動作し、意図した以上のX線が照射されたとしても、患者への危害が直ちに重傷につながることはない。
クラスCのSiMDは最も重要である。クラスCのSiMDは最もクリティカルなものであり、ソフトウェアの外部にある関連するリスク管理措置がすべて講じられた後でも、危険性があり、許容できないリスクにつながるアプリケーションが含まれる。クラスBとの違いは、結果として起こりうる危害が重傷または死亡を引き起こす可能性があるという点である。MRI検査に使用されるソフトウェアは、クラスCのSiMDの一例である。X線とは異なり、ソフトウェアの不具合によってMRIの放射線が許容レベルを超えた場合、患者は重傷を負ったり、死亡したりする可能性がある。
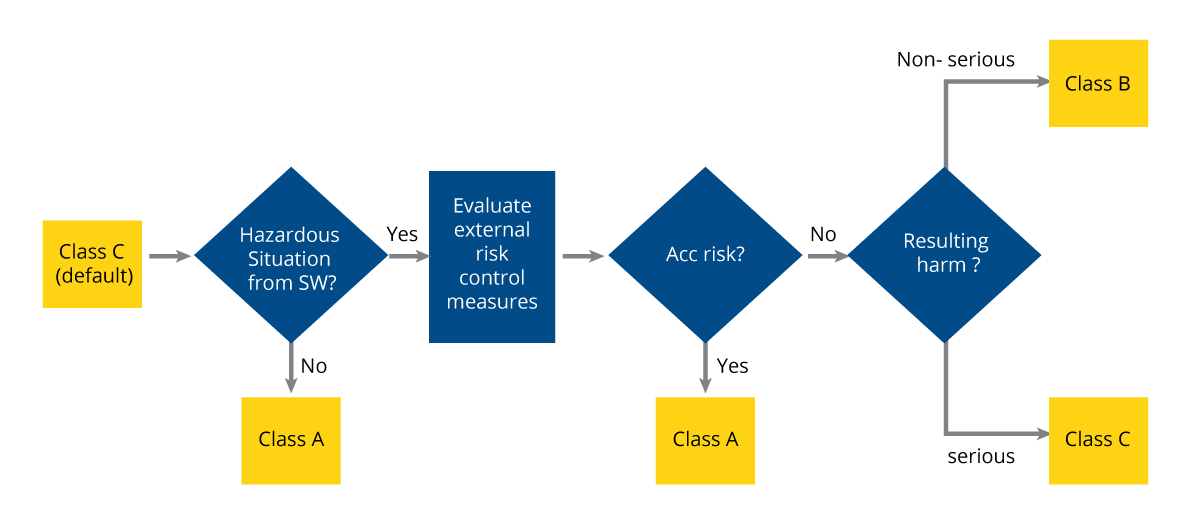
図1:SiMDの分類フローチャート
同様に、SaMDは、医療の現状とSaMDが医療の意思決定に提供する情報の重要性に基づいて、4つのカテゴリーに分類される。国際的な規制機関であるIMDRF(International Medical Device Regulators Forum)では、SaMDをI、II、III、IVに分類し、さらにa、bを加えて以下のように分類している:
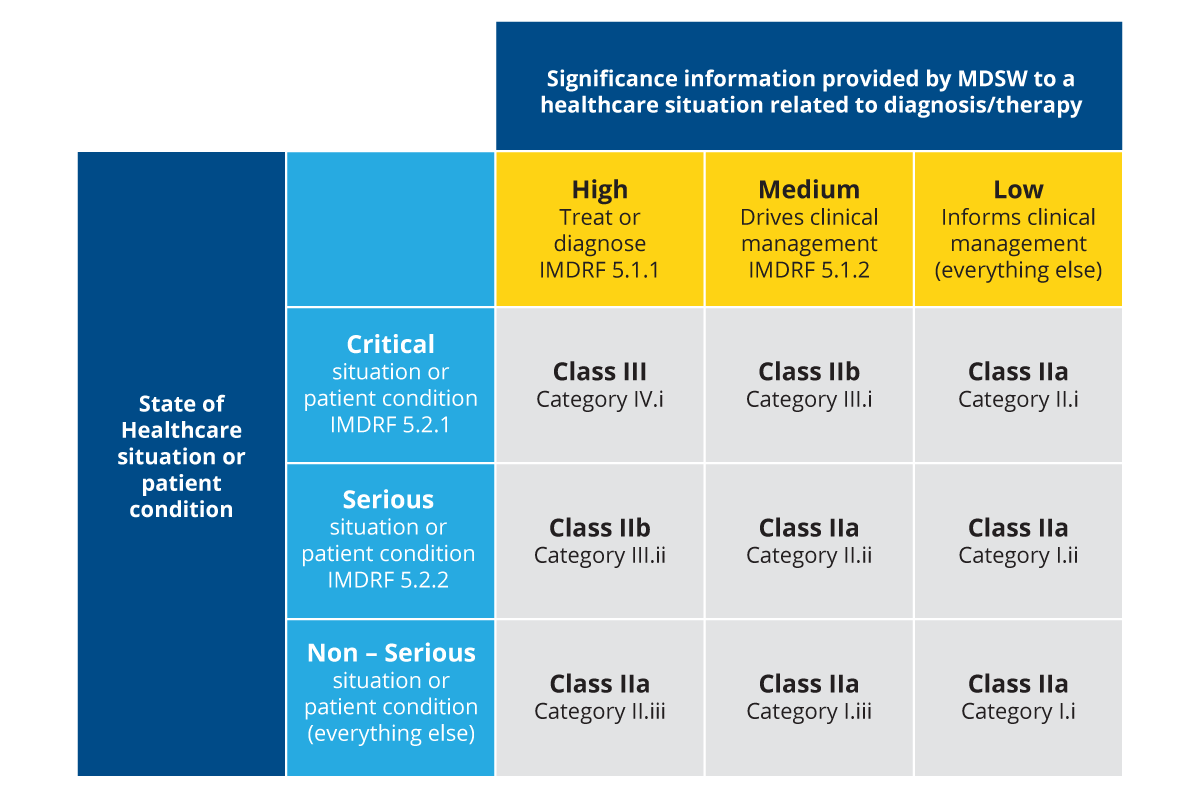
図2:SaMDのクラス
IEC 62304とIMDRFは、ソフトウェア開発ライフサイクルに干渉しない。そのため、開発プロセスは以下の段階と変わりません:
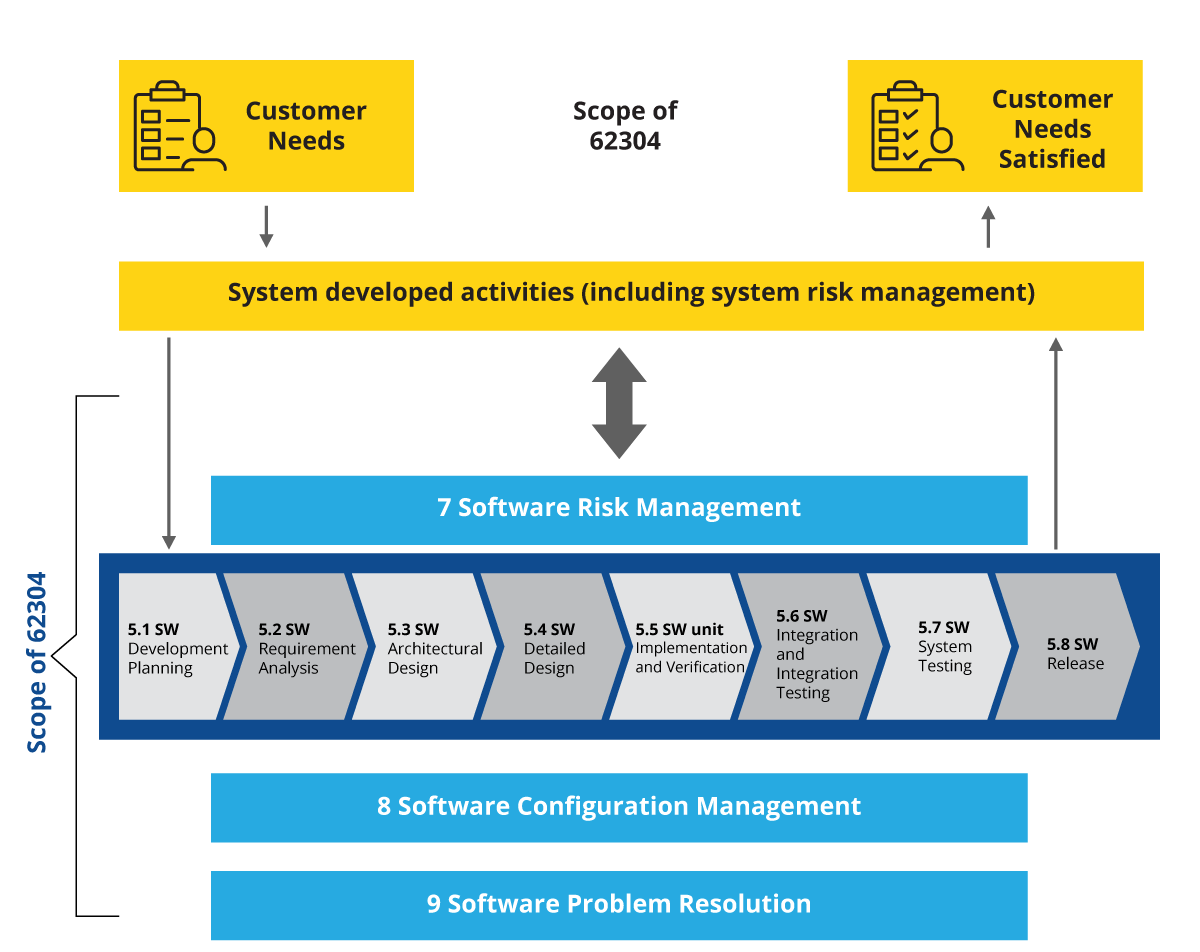
図 3: SDLC のステージを横断するリスク管理レイヤー
SaMDとSiMD開発の場合に必須である、SDLCのすべてのステージを横断する追加のレイヤーが1つだけあります。そのレイヤとは、ソフトウェアリスク管理である。IEC 62304 はソフトウェアリスク管理を強く強調しており、ソフトウェア会社はそれを遵守し、文書化し、証拠を示さなければならない。そこで、SiMD/SaMDとデバイスの分類に基づいて、特定の要素を文書化することが義務付けられている。各分類に必要な要素は以下の通り:
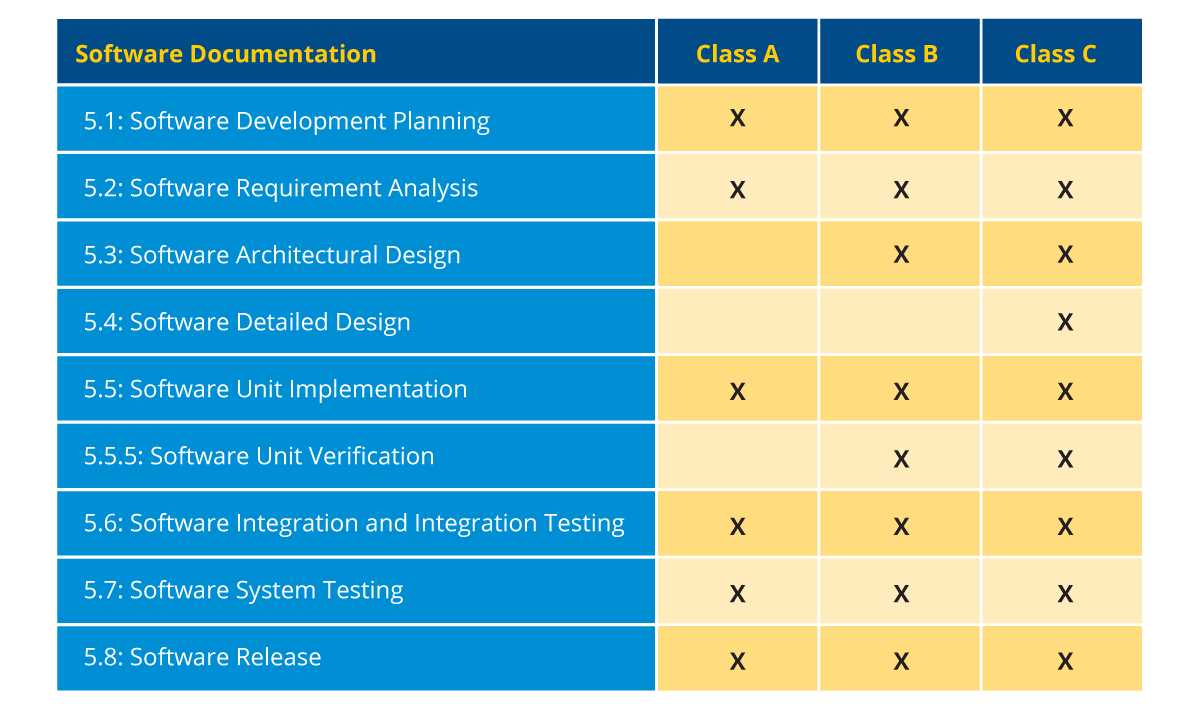
図4:ソフトウェアの分類に基づく文書化要件
SiMD/SaMDの開発とリリースに関連するIMDRFとIEC 62304のあらゆる側面に準拠することは、困難な努力となりうる。企業は多くの場合、既製のソフトウェアを選び、それをカスタマイズし、発売する医療機器に同梱して展開するつもりである。しかし、このアプローチでは、コンプライアンス違反による規制上のハードルに直面し、製品の発売が遅れるリスクがある。
そこでL&Tテクノロジー・サービス(LTTS)は、エンジニアリング・サービス提供における長年の経験と確かな能力で、専門家による介入とサポートを提供します。フォーチュン500に名を連ねる企業数社が、すでにLTTSに信頼を寄せています。分類の再評価から始まり、当該SiMD/SaMDが属するカテゴリの決定まで、あらゆる要件に対応します。ゼロからの開発であろうと、単に適用規格への準拠を保証するものであろうと、当社のソリューションはすべてをカバーします。
コンプライアンスを遵守し、医療機器の上市TATを短縮しましょう。私たちにできること、その方法をご覧ください。